ავტორი: ნინო შენგელია. კავკასიის საერთაშორისო უნივერსიტეტი მედიცინის ფაკულტეტი VI კურსის სტუდენტი.
საკვერცხის კიბო მსოფლიოს მასშტაბით საკმაოდ გავრცელებული ავთვისებიანი სიმსივნეა.ყოველწლიურად დიაგნოსტირებული ავთვისებიანი სიმსივნეების საშუალოდ 3,4%-ია, ხოლო კიბოს დიაგნოზით გარდაცვლილთა 4,7% საკვერცხის კიბოზე მოდის.
საკვერცხის ავთვისებიან სიმსივნეებს შორის ერთ-ერთ ყველაზე იშვიათ ფორმას საკვერცხის დაბალდიფერენცირებული სეროზული კარცინომა (LGSOC) წარმოადგენს, რომელიც უიშვიათეს ჰისტოლოგიურ ქვეტიპს მიეკუთვნება, ხასიათდება უნიკალური კლინიკური მიმდინარეობითა და სპეციფიკური მოლეკულური პროფილით, LGSOC საკვერხის სეროზული კარცინომების 2-5 %-ს შეადგენს, დაბალი გავრცელება განაპირობებს ინფორმაციისა და მიმდინარეობის სიმწირეს, თუმცა მაღალ ინტერესს .
მაღალდიფერენცირებული სეროზულ კარცინომასთან (HGSOC) შედარებით, LGSOC უფრო ახალგაზრდა ასაკში ვლინდება. დიაგნოსტირებული პაციენტების ასაკი 19 დან 79 წლამდე მერყეობს, საშუალო ასაკი 55,5 წელია. მიმდინარეობს ნელა და მიიჩნევა უკეთესი გადარჩენის პროგნოზით.(იხ. ცხრილი N1). მიუხედავად იმისა, რომ დიაგნოსტიკა უმეტეს შემთხვევაში შორსწასული სტადიების შემთხვევაში ხდება, 10 წლიანი სიცოცხლის ხანგრძლივობა II-IV სტადეიების შემთხვევაშიც კი 55%-ია. LGSOC გამოირჩევა მედიკამენტების მიმართ ძალიან დაბალი თერაპიული პასუხით, თუმცა FDA-ის მიერ გამოქვეყნებული უახლესი, 2025 წლის 8 მაისის ინფორმაციით ინოვაციური ორკომპონენტიანი მონოკლონური მედიკამენტის საშუალებით LGSOC-ის თერაპიული პასუხი 2-10% დან 44%-მდე გაიზარდა, რაც უდიდეს საშუალებას იძლევა სიმსივნისა და სიმპტომების მართვაში.
ცხრილი N1- 10 წლიანი გადარჩენის სიხშირე LGSOC და HGSOC დიაგნოსტირებუ პაციენტებში.
| LGSOC | HGCOS | |
| 10 წლიანი სიცოცხლის ხაგრძლივობა: I სტადია | 92% | 76% |
| 10 წლიანი სიცოცხლის ხაგრძლივობა: II-IV სტადია | 55% | 20% |
LGSOC-ის პათოფიზიოლოგია
საკვერცხის დაბალდიფერენცირებული სეროზული კარცინომა, განსხვავებით საკვერცხის სხვა სიმსივნეებისგან, არ ასოცირდება BRCA (Breast Cancer gene)გენის მუტაციასთან, ასევე პაციენტების ოჯახური ისტორია პირველი და მეორე რიგის ნათესავებში არ არის დატვირთული საკვერცხის კიბოს დიაგნოზით. LGSOC-ის ფორმირების მიზეზად ორი გზა არის მიჩნეული ინტრაოვარული და ექსტრაოვარული. ინტრაოვარულ მიზეზებს მიეკუთვნება უშუალოდ საკვერცხის ქსოვილოვანი მუტაცია, განსაკუთრებით ხშირია სეროზული ზღვრული სიმსივნის (SBT)ისტორია, პოლიკისტური საკვერცხე და მიულერის ცისტის არსებობა. ექსტრაოვარული მიზეზი გულისხმობს ფალოპის მილის ქსოვილთა ინვაგინაციას საკვერცხის ქსოვილში, მისი შემდგომი დიფერენცირებით, მუტაციითა და უმართავი ზრდით.
LGSOC-ის მოლეკულური მექანიზმი უშუალოდ MAPK (Mitogen-Activated Protein Kinase)-მიტოგენებით გააქტიურებული პროტეინკინაზის გზის მუდმივი აქტივაციის შდეგია.
MAPK გახლავთ სასიგნალო კასკადი , რომელიც უშუალოდ არის პასუხისმგებელი უჯრედთა პროლიფერაციაზე. MAPK-ის კასკადში ჩართულია უჯრედული ცილები Raf და Ras. უჯრედის მემბრანული თიროზინკინაზული რეცეპტორების აქტივაცია იწვევს მათ მიერ Ras ცილების გააქტიურებას და ხდება Ras-GTP კომპლექსის წარმოქმნა, რომელიც თავის მხრივ უკავშირდება სერინ/ტრეონინ-კინაზურ პროტეინკინაზა Raf-ს და მონაწილეობს მის ფოსფორილირებაში, გააქრიურებული Raf ცილა მოქმედებს MEK-ზე (თიროზინ/ტრეონინკინაზა) რომელიც ERK ცილის აქტივაციას იწვევს, ERK ცილა კი განიცდის ტრანსლოკაციას უჯრედის ბირთვში და ააქტიურებს ტრანსკრიფციის ფაქტორს, შესაბამისად ინდუცირდება დნმ-ს რეპლიკაცია. ზემოთხსენებული ჯაჭვური მექანიზმი გახლავთ უჯრედის დაყოფის მოლეკულური გზა, მოცემულ ჯაჭვში Ras და Raf-ის ჭარბი ექსპრესია იწვევს MAPK გზის მუდმივ აქტივაციას რისი შედეგიც არის უჯრედთა უჯონტროლო ზრდა და გაყოფა, ყოველივე ეს კი იწვევს საკვერცხის დაბალდიფერენცირებული სეროზული კიბოს წარმოქმნას.
David M. Gershenson –ის მიერ 2021წელ გამოქვეყნებული კვლევის მიხედვით შესწავლილი იქნა LGSOC ის დიაგნოზის მქონე 215 პაცინტი, მათგან 140-ს ჰქონდა 1 და მეტი მუტაცია, 75 პაციენტში მუტაცია ვერ აღმოაჩინეს. კვლევაში მონაწილე პაციენტებს არანორმალურად ჭარბი რაოდენობით აღენიშნებათ Ras და Raf ცილები, რისი საფუძველიც გახლდათ Ras ცილის გენების,KRAS და NRAS და Raf ცილის BRAF გენის მუტაციები. ამათგან შემთხვევათა 33% მოდის KRAS მუტაციაზე, 11,8 % NRAS მუტაციაზე,ხოლო 8,4% BRAF მუტაციაზე.
(ცხრილი N1)
| გენის მუტაცია | გენის პროდუქტი | პაციენტთა პროცენტულობა(215 პაციენტიდან) |
| KRAS | Ras | 33% |
| NRAS | Ras | 11,8 |
| BRAF | Raf | 8,4 |
| BRAF | Raf | 8,4 |
ცხრილი N2
Dr.Dane Cheasley-ის მიერ 2023 წელს გამოქვეყნებული კვლევის მიხდვით 71 პაციენტს ჩაუტარდა ღრმა გენომური კვლევა და დადასტურდა, რომ KRAS,NRAS და BRAF მუტაციებთან ერთად გვხვდება მუტაციები შემდეგ გენებში USP9X-11,2%-,MACF1-11,2%, ARIDA-9,9%, CDKN2 -5,6%
( ცხრილი N2).
ზემოთხსენებული ორი კვლევა თვალნათლივ გვიჩვენებს MAPK გზისა და სიმსივნის სუპრესორი გენების მუტაციის სიხშირეს LGSOC პაციენტებში, ასევვე უნდა აღინიშნოს ის ფაქტი, რომ პაციენტებს, რომელთაც კოლორექტალური, ფილტვის და პანკრეასის KRAS სიმსივნეები აქვთ, მათ LGSOC-ის ფორმირების რისკი ეზრდებათ.
| გენის მუტაცია | გენის პროდუქტი | პაციენტთა პროცენტულობა(215 პაციენტიდან) |
| USP9X | TGF-B(სიმსივნის ზრდის ფაქტორი ბეტა) | 11.2% |
| MACF1 | Microtubule-actin crosslinking factor1(მიკროტუბული აქტინური ცილა) | 11.2% |
| ARID1A | BAF(ავტოანტიგენური ბარიერის ფაქტორი) | 9.9% |
| NF2 | სიმსივნის სუპრესორი გენი | 4.2% |
| DOT1L | ჰისტონმეთილტრანსფერაზა | 5.6% |
| ASH1L | ჰისტონმეთილტრანსფერაზა | 4.2% |
| CDKN2 | სიმსივნის სუპრესორი გენი | 9.9% |
ცხრილი N3
ჰისტომოფოლოგია
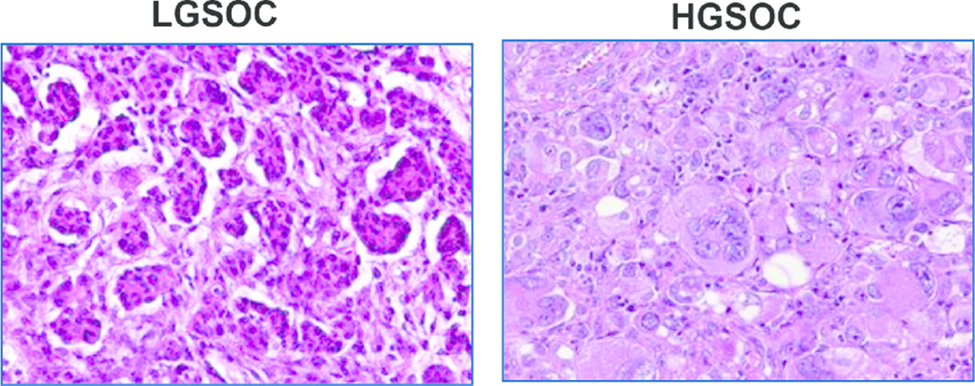
LGSOC ჰისტოლოგურად წარმოდგენილია მონოტონური, კუბური მცირედ ეოზინოფილური უჯრედების სახით, ატიპია მერყეობს მუბუქიდან-საშუალომდე,ხოლო მიტოზების რაოდენობა არ აღემატება 12 მიტოზს 10 HPF(მაღალი გამადიდებელი) ველის ფარგლებში – რაც დაბალი პროლიფერაციული აქტივობის მაჩვენებელია.
სიმპტომები
LGSOC ხშირად გამოირჩევა მდორე კლინიკური მიმდინარეობით და საწყის ეტაპზე სიმპტომები არ ახასიათებს ან იშვიათად ვლინდება, თუმცა, დროთა განმავლობაში სიმსივნე პროგრესირებს და იწვევს სპეციფიკურ და არასპეციფიკურ სიმპტომებს.
სიმპტომებს გამოყოფნ შემდეგ ტიპებად:
მენსტრუალური და რეპროდიქტიული სისტემისმრივი
- დისმენორეა;
- ამენორეა;
- მენორაგია;
- უნაყოფობა.
საჭმლის მომნელებელი სისტემისმხრივი :
- მადის დაკარგვა;
- გულისრევა;
- შეკრულობა ან შარდვის გაძნელება (თუ სიმსივნე მეზობელ ორგანოებს აწვება);
მუცლის ღრუს ორგანოების კომპრესიის ნიშნები:
- მუცლის ტკივილი ან დისკომფორტი;
- მუცლის მოცულობის ზრდა;
- ადვილად დანაყრება ;
- მუცლის დაჭიმულობა;
- ასციტი;
სისტემური სიმპტომები (დამახასიათებელია მეტასტაზებისას):
- დაღლილობა;
- წონაში კლება;
- ტემპერატურის მატება;
- დისპნეა.
აღსანიშნავია ის ფაქტი, რომ LGSOC ის სიმპტომები თავს იჩენს შორსწასული ფორმების დროს, განსვავებით HGSOC-გან, შესაბამისად დიაგნოსტირებული შემთხვევების უდიდეს ნაწილში LGSOC-ის გვიანი სტადიები გვხვდება ხოლო HGSOC-ის ადრეული სტადიები.
ყველაზე ხშირი სიმპტომები მენსტრუალური ციკლის დარღვევასთან ასოცირდება, სიმსივნის ზომაში ზრდასთან ერთად კი სისტემური სიმპტომების გამოვლენა იმატებს. მუცლის ღრუს ორგანოებზე სიმსივნური მასის ზეწოლის შედეგად წნევის გაზრდის ფონზე ხშირია სუნთქვის უკმარისობა, გულისრევა და ღებინება ,ნაწლავების ობსტრუქცია, დიზურია ან ანურია, ამიტომ ხშირად პაციენტი არა გინეკოლოგს, არამედ გასტროენტეროლოგს მიმართავს.
LGSOC-ის სტადირება
| I სტადია | ლოკალიზებულია მხოლოდ საკვერცხეებში-მხოლოდ ერთ საკვერცხეში ან ბილატერალურად. |
| II სტადია | კიბოს უჯრედები გავრცელებულია მცირე მენჯის ახლომდებარე ორგანოებზე:ფალოპის მილებსა და საშვილოსნოზე. |
| IIIსტადია | კიბოს უჯრედები გვხვდება მცირე მენჯის ღრუს გარეთ(მუცლის ღრუს ორგანოებში) ახლომდებარე ლიმფურ კვანძებში, ღვიძლში, ნაწლავებში. |
| IV სტადია | შორეული მეტასტაზები მუცლის ღრუს გარეთ. |
დიაგნოსტირება
ულტრასონოგრაფია: საკვერცხის დაბალდიფერენცირბული სეროზული კარცინომის დიაგნოსტიკის ერთ-ერთი მნიშვნელოვანი მეთოდი ულტრასონოგრაფიაა, ადრეული სავარაუდო დიაგნოზის დასასმელად, ჰისტომორფოლოგიამდე მისი გამოყენება ბევრ ინფორმაციას იძლევა. ულტრასონოგრაფიულად შესაძლოა დავინახოთ საშუალო დონის რთული ცისტური წარმონაქმნები მყარი კომპონენტებითა და კალციფიკაციებით. იშვიათად არის მჭიდროდ ვასკულარიზებული, რაც გამიჯვნის საშუალებას იძლევა HGSOC-გან.
კომპიუტერული ტომოგრაფია: CT მეტასტაზების შეფასებასა და დიაგნოსტიკაში ძირითად გამოსახულებით მეთოდად მოიაზრება, იდეალურად შეგვიძლია ლიმფადენოპათიისა და პერიტონეალური მეტასტაზების ამოცნობა(სიზუსტე 89%), CT-ზე LGOSC ვიზუალიზდება, როგორც დიდი, კომპლექსური კარგად შემოსაზღვრული ცისტური წარმონაქმნი პაპილარული გამონაზარდებით და მყარი კომპონენტებით,შეიძლება იყოს უნილატერალური ან ბილატერალური. ხშირად აღინიშნება კალციფიკაციები როგორც ადნექსალურ მასაში, ასევე პერიტონეალურ მეტასტაზებში.
მაგნიტო-რეზონანსული ტომოგრაფია:MRI არის უმნიშვნელოვანესი ინსტრუმენტი LGSC-ის დიფერენცირებისთვის სხვა ადნექსალური მასებისგან, მაგალითად:
- LGSOC აქვს უფრო დაბალი ADC(apparent diffusion coefficient), ვიდრე SBT-ს, რაც მეტყველებს უფრო მეტ ცილოვან/ცხიმოვან კომპონენტზე და უჯრედულობაზე.
- უფრო მაღალი ADC, ვიდრე HGSC-ს (HGSC როგორც წესი უფრო უჯრედული და აგრესიულია, რაც ზრდის წყლის მოძრაობის შეზღუდვას და ამცირებს ADC-ს)
PET სკანირება: PET LGSOC-ის ადრეულ დიაგნოსტიკაში არ გამოიყენება, ვინაიდან ფლუროდეოქსიგლუკოზა(FDG) შესაძლოა დაგროვდეს ნაწლავში, ან საკვერცხის კეთილთვისებიან ცისტაში და ცრუდადებითი ეფექტი მოგვცეს, ასევე LGSOC და HGSOC-ის დიფერენციაციას PET-ით ვერ მოვახერხებთ, ვინაიდან FDG-ს ჩართვა ორივე წარმონაქმნში თანაბრად ხდება,მაგრამ,ზემოთხსენებულის მიუხედავად რეციდივის გამოვლენაში PET/CT ხშირად გამოყენებადი კვლევაა.
სიმსივნის მარკერი: CA-125 მაღალი(>35U/ml) აღმოჩნდა LGSOC-დიაგნოზის მქონე პაცინტთა 84%-ში, თუმცა როგორც სადიაგნოსტიკო კრიტერიუმს მას ნაკლებად გამოიყენებენ და უფრო დიდი ყურადღება ენიჭება მკურნალობის განსაზღვრასა და ტაქტიკის შერჩევაში. თუ სიმსივნე მკურნალობას ექვემდებარება CA-12-ს რაოდენობა იკლებს.
ჰისტომორფოლოგიური კვლევა: როგორც ზემოთ არის აღნიშნული, LGSOC-ის ჰისტომორფოლოგიური სურათი მკვეთრად განსხვავდება საკვერცხის სხვა ტიპის სიმსივნეებისგან, ამიტომ ჰისტომორფოლოგიური კვლევა სავარაუდო დიაგნოსტიკის დადასტურების იდეალური საშუალებაა.
მკურნალობა
ქირურგიული მკურნალობა
LGSOC მკურნალობის პირველი საფეხური ქირურგიული მკურნალობაა, თუ ქალი ფერტილურია და სიმსივნე არ სცდება I სტადიას (Ia,IC) ამ შემთხვევაში შესაძლებელია ფერტილობის შემანარჩნებელი ქირურგიული ჩარევის ჩატარება (Fertility-Sparing Surgery – FSS) რაც გულისხმობს მხოლოდ ერთი დაზიანებული საკვერცხის ამოკვეთას შემდგომი კონტროლით. II სტადიიდან კი აუცილებელია ჰისტერექტომია დანამატებთან ერთად ლიმფადენექტომიით და შემდგომი კონტროლით.
მედიკამენტური მკურნალობა
როგორც ზემოთ იყო ნახსენები LGSOC გახლავთ ის უნიკალური სიმსივნე, რომელიც არ ექვემდებარება მედიკამენტურ თერაპიას, ნეოადიუვანტური ქიმიოთერაპიის მიმართ LGSOC-ს ბიოლოგიური პასუხი თითქმის არ აქვს 0-2%, რაც თერაპიის საჭიროებაზე ეჭვბს ბადებს, ადიუვანტური თერაპია კი 2020 წლამდე მოიცავდა პლატინის პრეპარატებს (კარბოპლატინი )და ბევაციზუმაბს თუმცა 2018 წლის მონაცემებით პლატინასენსიტიური პაციენტების თერაპიაზე პასუხის მაჩვენებელი ORR( Overall Response Rate)4%-ს არ აღემატებოდა, მევაციზუმაბის (2023 წლის მიხედვით) ORR- 40%-მდეა,სიცოხლის ხაგრძლივობას ზრდის საშუალოდ 21-33 თვით,მაგრამ, გასათვალისწინებელია მევაციზუმაბის არასასურველი გვერდითი ეფექტების სიჭარბე და რეციდივების გამოვლენის სიხშირე.
ჰორმონული თერაპია LGSOC-ის დროს გამოიყენება, როცა სიმსივნე ესტროგენულ რეცეპტორებს შეიცავს( არსებობს შემთხვევები, როცა ესტროგენული რეცეპტორები არ გვხვდბა). თერაპია მოიცავს ანტიესტროგენულ მედიკამენტებს, რომელთა საშუალებითაც სიმსივნის ზომაში ზრდას ვაფერხებთ. ჰორმონული მედიკამენტები შესაძლოა გამოყენებული იქნას როგორც ძირითად მკურნალობის სქემაში ქიმიოთერაპიასთან ერთად, რეციდივების მართვის დროს, ასევე შემანარჩუნებელი თერაპიის სახითაც. ჰორმონოთერაპია მოიცავს ძირითად სამი ტიპის მედიკამნტს:
- არომატაზის ინჰიბიტორები (AIs) :Letrozole (ლეტროზოლი),Anastrozole (ანასტროზოლი),Exemestane (ექსემესტანი) ეს პრეპარატები აინჰიბირებენ არომატაზას, ფერმენტს, რომელიც ანდროგენებს ესტროგენად გარდაქმნის. უმეტესად გამოიყენება მენოპაუზის შემდგომ ქალებში.
- სელექციური ესტროგენის რეცეპტორის მოდულატორები (SERMs) სელექტიურად ბლოკავენ ესტროგენის რეცეპტორებს სიმსივნურ უჯრედებში, ერთ ერთი წარმომადგენელია Tamoxifen (ტამოქსიფენი).
- მალუთეინიზირებელი ჰორმონის რილიზინგ ჰორმონის აგონისტები (LHRH agonists)
თავდაპირველად ეს მედიკამენტები მოქმედებენ ჰიპოფიზზე და ასტიმულირებენ მალუთინიზირებელი და ფოლიკულომასტიმულირებელი ჰორმონების გამოყოფას რის შედეგადაც , დროებით იზრდება ესტრადიოლის წარმოქმნა, თუმცა ხანგრძლივი სტიმულაციის ფონზე ჰიპოფიზის რეცეპტორების დესენსიტიზაცია და დაუნრეგულაცია ხდება, რისი შედეგიც არის ფოლიკულომასტიმულირებელი და მალუთეინიზირებელი ჰორმონების პროდუქციის დონის ვარდნა, შესაბამისად საკვერცხეში ესტროგენების სინთეზის მკვეთრი შემცირება.ძირითადი მედიკამენტებია Leuprolide (ლეუპროლიდი) და Goserelin (გოსერელინი), უმეტესად გამოიყენება პრემენოპაუზურ ქალბში.
საბოლოო ჯამში LGSOC-ის ჰორმონული თერაპის საშუალო ORR არის 12-25%., როცა HGSOC-ის ORR ჰორმონულ თერაპიაზე 80%-ს აღწევს.
2025 წლის 8 მაისს (საკვერცხის კიბოს დღე) FDA-მ გამოაქვეყნა ინფორმაცია , ინოვაციური კომბინირებული მონოკლონური თერაპიის შესახებ, რომელიც გამოიყენება LGSOC-ის მკურნალობისთვის , ეს მედიკამენტები გახლავთ Avmpaki Fakzynja, რომელიც მოიცავს avutometinib+defactinib-ს (MEK 1 და FAK ინჰიბიტორებს). როგორც ზემოთ არის ნახსენები LGSOC-ის პათოგენეზი MAPK სასიგნალო გზას მოიცავს, რაშიც ჩართულია MEK (თიროზინ/ტრეონინკინაზა)რომელიც მონაწილეობს ERK ცილის აქტივაციაში და დნმ-ს რეპლიკაციაში, სტატისტიკური მონაცემების მიხედვით პაციენტთა უმეტესობას KRAS მუტაცია აღენიშნება რაც Ras ცილის ჭარბ ექსპრესიას და მის მიერ MEK-ის მუდმივ აქტივაციას უწყობს ხელს, შესაბამისად უჯრედების დაყოფის პროცესი ანომალურად ჩქარდება. Avutometinib გახლავთ ის მედიკამენტი რომლებიც უშუალოდ MEK ცილის ინჰიბირებას ახდენს, MEK-ის გააქტიურება Ras-Raf-ით ვეღარ ხდება რაც შემდგომში დნმ-რეპლიკაციას თრგუნავს, საბოლოოდ კი ვიღებთ უჯრედთა გაყოფის შეჩერებას, თუმცა მნიშვნელოვანია ის ფაქტი, რომ პაციენტებში, რომლებსაც მხოლოდ MEK ინჯიბიტორებს აძლევდნენ აღინიშნა FAK თიროზინკინაზის (Focal Adhesion Kinase) გააქტიურება, რაც სიმსივნის წამლის მიმართ რეზისტენტობას აძლიერებს, ვინაიდან FAK მოქმედებდა როგორც MEK და სიმსივნური უჯრედები კვლავ აგრძელებდნენ გამრავლებას, ამიტომაც Avutometinib-თან ერთად ახალ თერაპიაში defactinib-ს გამოიყენებენ, რაც FAK-ის დაბლოკვის შედეგად შეამცირებს სიმსივნის რეზისტენტობას თერაპიის მიმართ და გაახანგრძლივებს სიცოცხლის ხანგრძლივობას. აღსანიშნავია ის ფაქტი, რომ avutometinib+defactinib-ის თერაპიაზე პასუხის მაჩვენებელი ORR-44%-ია რაც ძალიან სასიხარულო შედეგია, თუ გავითვალისწინებთ იმას, რომ სიცოცხლის ცანგრძლივობასაც საშუალოდ 33 თვით ზრდის და სერიოზული გვერდითი ეფექტების გამოვლენის სიხშირე სხვა მონოკლონურ ანტისხეულებთან შედარებით ნაკლებია.
LGSOC-ის დიაგნოზი ორსულ პაციენტში -უიშვიათესი ქეისი.
რაგდგან LGSOC იშვიათ სიმსივნეებს მიეკუთვნება , თითქმის არ ხდება მისი დიაგნოსტირება ორსულ პაციენტებში. 2023 წელს Mariana abduch rahal-ის და მისი კოლეგების მიერ გამოქვეყნებულ ქეისში სწორედ ასეთ იშვიათ შემთხვევაზეა მოთხრობილი.
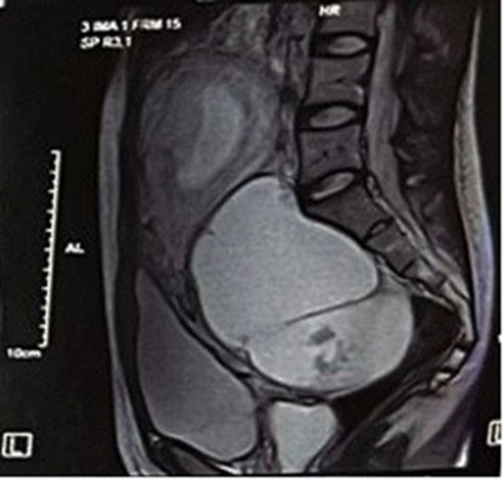
26 წლის ორსულმა პაციენტმა მიმართა გინეკოლოგიურ განყოფილებას, საკვერცხეზე დიაგნოსტირებული წანაზარდის გამო. ულტრასონოგრაფიულად გამოვლინდა დიდი ზომის (122მმ*104მმ*90მმ)ჰეტეროგენული წარმონაქმნი, ვასკულარიზებული კედლებით.MRI-ზე ვიზუალიზდა მარჯვენა საკვერცხის ცისტური წანაზარდი და დაიგეგმა ოპერაცია. ლაპარატომიული მიდგომით 27-ე კვირაზე განხორციელდა მარჯვენამხრივი სალფინგოოფორექტომია, მასალის ჰისტოპათოლოგიური კვლევით გამოვლინდა LGSOC, ლიმფოვასკულარული ინფილტრაციის გარეშე. მშობიარობა 36-ე კვირას ჩატარდა გართულებების გარეშე და 46-ე დღეს დაიგეგმა ლაპარასკოპიული კვლევა, რის შედეგადაც აღებულ ბიოფსიურ მასალებში სიმსივნური უჯრედები არ გამოვლინდა. პაციენტის რეაბილიტაცია და მკურნალობა დამაკმაყოფილებლად მიმდინარეობს რეციდივების ნიშნების გარეშე.
საკვერცხის დაბალდიფერენცირებული სეროზული კარცინომა უიშვიათესი და განსაკუთრებული ჰისტომორფოლოგიური და მოლეკულური პატერნების მქონე სიმსივნეა, რომელიც რთულად ემორჩილება მედიკამენტურ მკურნალობას, თუმცა უახლესი მონაცემების მიხედვით MEK+FAK ბლოკატორების საშუალებით შესაძლებელია მისი მართვა, დღეს-დღეობით კი ვრწმუნდებით , რომ კიბო განაჩენი არ არის, მედიცინის განვითარებასთან ერთად ნელ-ნელა იმსხვრევა მითებიც კიბოს უძლეველობის შესახებ.
- https://pmc.ncbi.nlm.nih.gov/articles/PMC5365187/
- https://pubmed.ncbi.nlm.nih.gov/35443055/
- https://pubmed.ncbi.nlm.nih.gov/28221866/
- https://www.international-journal-of-gynecological-cancer.com/article/S1048-891X(24)01689-X/fulltext
- https://www.sciencedirect.com/science/article/pii/S0305737222001736
- https://www.fda.gov/drugs/resources-information-approved-drugs/fda-grants-accelerated-approval-combination-avutometinib-and-defactinib-kras-mutated-recurrent-low
- https://investor.verastem.com/news-releases/news-release-details/fda-approves-avmapkitm-fakzynjatm-combination-therapy-first-ever
- https://www.uptodate.com/contents/management-of-low-grade-serous-carcinomas-of-the-ovary/abstract/21
- https://pmc.ncbi.nlm.nih.gov/articles/PMC9951382/
- https://www.researchgate.net/figure/Trends-of-LGSOCs-all-stages-Dots-represent-proportion-of-LGSOC-at-given-year-and-bars_fig1_322166788
- https://www.sciencedirect.com/topics/biochemistry-genetics-and-molecular-biology/kras#:~:text=KRAS%20is%20the%20most%20commonly%20mutated%20oncogene%20in%20human%20cancer,forms%20of%20the%20KRAS%20oncoprotein.
- https://pmc.ncbi.nlm.nih.gov/articles/PMC9669513
- https://www.uchicagomedicine.org/cancer/types-treatments/ovarian-cancer/low-grade-epithelial-ovarian-cancers
- https://www.international-journal-of-gynecological-cancer.com/article/S1048-891X(24)10684-6/fulltext